Alanina
Definición, función biológica en el cuerpo, dónde se encuentra, fórmula, características, estructura molecular, importancia, beta alanina, alimentos que la contienen, usos.
 |
Apariencia y propiedades de la alanina
En su forma pura, la alanina es un polvo blanco soluble en agua. El punto isoeléctrico de la alanina se da a pH 6,00. Las constantes de ácido son las siguientes: pKa1 (carboxilo) a 2,34 y pKa2 (grupo amina) a 9,69.
La L-alanina se crea en las células musculares a partir del glutamato, en un proceso llamado transaminación. En el hígado, la alanina se convierte en piruvato. Además, la alanina aminotransferasa (ALT) cataliza la reacción en la que el grupo amino de la alanina se transfiere al α-cetoglutarato.
Buenas fuentes de alanina son la carne, el pescado y los huevos, así como algunas plantas ricas en proteínas como los aguacates.
Los estudios en animales han demostrado que la alanina tiene un efecto reductor del colesterol. Las personas con síndrome de fatiga crónica tienen mayor cantidad de alanina y valores bajos de tirosina y fenilalanina.
En la glucólisis anaeróbica, la alanina es secretada por los músculos. Sin embargo, la cantidad encontrada es mucho mayor de lo que se puede explicar por la descomposición de las proteínas musculares. En el músculo, los grupos amino de los aminoácidos pueden ser transferidos a piruvato a través de una transaminación. Esto permite que el nitrógeno, que se libera durante la degradación de las proteínas musculares, se elimine de forma segura. Por consiguiente, la carga metabólica del músculo es, por así decirlo, empujada hacia el hígado. En el hígado, la alanina se convierte de nuevo en glucosa y el nitrógeno liberado se descarga en forma de urea.
Estructura de la alanina
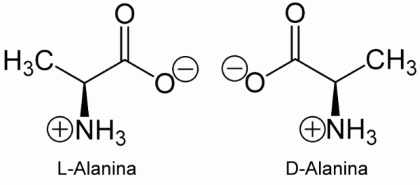 |
La alanina es, después de la glicina, el aminoácido más simple. El grupo residual es un grupo metilo y, por lo tanto, la alanina se clasifica como un aminoácido no polar.
Ambos enantiómeros, la D-alanina y la L-alanina, se producen de forma natural, aunque la D-alanina se encuentra solo en la pared celular de ciertas bacterias. La D-alanina está particularmente involucrada en la construcción de peptidoglicano, el principal constituyente de la pared celular bacteriana. La D-alanina se forma a partir de L-alanina por la acción de una enzima isomerasa, la alanina racemasa.
La beta-alanina es ácido 3-aminopropanoico o ácido-β aminopropanoico, un isómero posicional de la alanina. En esta molécula, el grupo amino está en la posición β (3) del grupo carboxilo, y en la posición α sobre la alanina.
Funciones de la alanina
Cuando forma parte de una proteína, la alanina no es un aminoácido muy reactivo debido a la limitada reactividad del grupo metilo en condiciones fisiológicas. Por eso es una opción al hacer estudios de mutagénesis dirigida, que se usan para revelar la función de un aminoácido más reactivo (la sustitución de éste por alanina permite la existencia de un aminoácido en la cadena polipeptídica pero sin función de reacción).
A pesar de su baja reactividad química, la alanina puede tener funciones de reconocimiento de sustratos o reguladores alostéricos en sitios activos o de regulación de enzimas.
La alanina actúa en el metabolismo del triptófano y de la vitamina piridoxina, en la síntesis de proteínas y en la gluconeogénesis. Además, la alanina también actúa como transportador de los iones de amonio producidos en los músculos hacia el hígado, mediante la aminación de piruvato en alanina, con el transporte posterior de la alanina hasta el hígado y la desaminación de la alanina por reacción con alfa-cetoglutarato (transaminación), formando como productos glutamato (que se utiliza en el ciclo de la urea) y piruvato de nuevo.
Síntesis de la alanina
Biosíntesis
La alanina es codificada genéticamente por los codones GCU, GCC, GCA, y GCG.
La síntesis bioquímica más importante de alanina en el cuerpo se lleva a cabo a través de una aminación reductora del ácido pirúvico. La alanina es muy fácil de hacer y su ruta de síntesis se ha relacionado con otros procesos bioquímicos importantes tales como la glucólisis, la gluconeogénesis y el ciclo del ácido cítrico (ciclo de Krebs). Además, la alanina puede obtenerse a partir de otros aminoácidos no polares ramificados como la valina, la leucina y la isoleucina.
Síntesis química
La L-alanina fue sintetizada en 1850 por Adolph Strecker, que eligió el nombre "alanina" al ser un derivado del nombre "aldehído", ya que la sintetizó a través de esta sustancia. En 1888, T. Weyl obtuvo alanina a través de un componente de la proteína de la seda llamado fibroína. La fibroína de seda contiene aproximadamente un 29,7% de L-alanina.
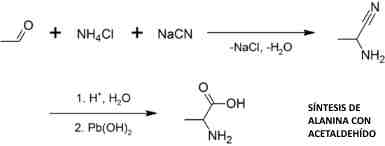
Una mezcla racémica de D- y L-alanina se puede preparar mediante la síntesis de aminoácidos de acetaldehído con cloruro de amonio, en presencia de cianuro de sodio:
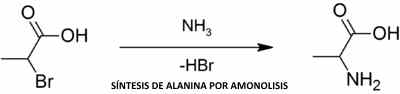
Un método alternativo es la amonolisis de ácido 2-bromo propanoico: